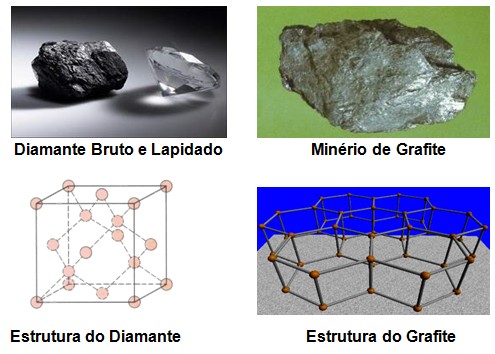
Feldspato (do alemão feld, campo; e spat, uma rocha que não contém minério) é o nome de uma importante família de minerais, do grupo dos tectossilicatos, constituintes de rochas que formam cerca de 60% da crosta terrestre. Cristalizam nos sistemas triclínico ou monoclínico.
Eles cristalizam do magma tanto em rochas intrusivas quanto extrusivas; os feldspatos ocorrem como minerais compactos, como filões, em pegmatitas e se desenvolvem em muitos tipos de rochas metamórficas. Também podem ser encontrados em alguns tipos de rochas sedimentares.O perfeito entendimento das relações entre os feldspatos apenas é atingido com a caracterização química e estrutural, aspectos dependentes da temperatura e pressão de cristalização e da história termal e de formacional subsequente. Ele pode ser de alta temperatura quando preserva a estrutura de geração a alta temperatura e de baixa temperatura quando as estruturas de alta temperatura sofrerem modificação lenta e total para formas de baixa temperatura, ou quando cristalizar em ambiente de baixa temperatura (cristalização plutônica). Os feldspatos podem ocorrer também em estados estruturais correspondentes a temperaturas intermediárias.
Os Feldspatos representam o mais abundante grupo de minerais constituintes das rochas ígneas. Podem ocorrer em rochas que sofreram metamorfismo térmico ou regional e também são importantes constituintes de muitos sedimentos e rochas sedimentares.
São uma combinação química entre silicatos de alumínio com potássio, sódio, cálcio e, raramente, bário. Devido a sua grande complexidade química e extraordinária presença na crosta terrestre serve de base para a classificação das rochas ígneas.
Dureza: Varia entre 6 e 6,5 (Escala de Mosh).
Densidade: 2.55 e 2.76 g/cm³.
Clivagem: Perfeita em duas direções, formando angulo de 90º (ou próximo disto).
Brilho: Vítreo.
Sistema de Cristalização: Monoclínico, triclínico.
Aspecto: Translúcido e transparente.
Traço: Branco.
Fratura: Desigual, estilhaçada, granulada.
Chakra: Primeiro Raiz
Energia: Amor e amizade
Os feldspatos possuem numerosas aplicações na indústria, devido ao seu teor em álcalis e alumina. As aplicações são:
Fabrico de vidro (sobretudo feldspatos potássicos; reduzem a temperatura de fusão do quartzo, ajudando a controlar a viscosidade do vidro).
Fabrico de cerâmicas (são o segundo ingrediente mais importante depois das argilas; aumentam a resistência e durabilidade das cerâmicas).
Como material de incorporação em tintas, plásticos e borrachas devido à sua boa dispersibilidade, por serem quimicamente inertes, apresentarem pH estável, alta resistência à abrasão e congelamento e pelo seu índice de refracção (nestas aplicações usam-se feldspatos finamente moídos).
Produtos vidrados, como louça sanitária, louça de cozinha, porcelanas para aplicações eléctricas.
E ainda, em eléctrodos de soldadura, abrasivos ligeiros, produção de uretano, espuma de látex, agregados para construção...
Feldspato também serve como enfeite.
As reservas Brasileiras de feldspato totalizam aproximadamente 116 milhões de toneladas, sendo 41,4% reservas medidas, 28% reservas indicadas e 30,6% reservas inferidas. Entre os estados brasileiros destacamos São Paulo com 47,1%, Minas Gerais com 36,3% e o Paraná com 10,7% das reservas nacionais. Analisando por regiões estaduais temos os municípios de Castro – PR, com 11 milhões, Sorocaba – SP com 7,7 milhões e Itinga – MG com 4,2 milhões de toneladas. Com relação às reservas de feldspato, existe uma grande dificuldade para uma quantificação mais precisa, uma vez que ele ocorre em rochas pegmatíticas.
Fonte: CPRM
 Indicadores Econômicos1 hora atrás (25.06.2019 15:35)
Indicadores Econômicos1 hora atrás (25.06.2019 15:35) © Reuters. (Blank Headline Received)
© Reuters. (Blank Headline Received)